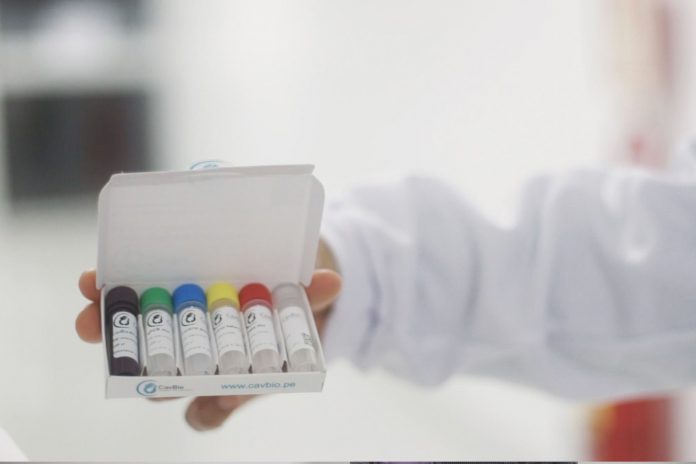
Buena noticia. El Perú ya cuenta con el primer kit de bajo costo desarrollado, producido y comercializado en nuestro país a fin de atender de forma rápida y oportuna la demanda nacional por este tipo de pruebas de alta efectividad. La empresa BTS Consultores obtuvo el registro sanitario para CavBio.
Próximo objetivo es lograr la exportación del kit CavBio a otros países de la región
En el 2020, este proyecto fue uno de los 42 ganadores del Reto InnovaCovid-19, convocado por ProInnóvate a inicios de la pandemia, por lo que recibió el cofinanciamiento de 450 mil soles para su validación clínica y comercial y empaquetamiento, basado en protocolos científicos probados recomendados por la Organización Mundial de la Salud (OMS) y los Centros para el Control y Prevención de Enfermedades de los EE.UU. (CDC).
Leer también [¡Atención! Hoy y mañana habrá corte de luz en Lima y Callao]
Durante 10 meses de trabajo, BTS Consultores logró validar in vitro y clínicamente el kit CavBio con muestras nacionales provistas por el Instituto Nacional de Salud (INS) y muestras internacionales provistas por la Organización PATH-USA, además de gestionar y lograr que laboratorios autorizados, tanto públicos como privados, validaran el kit en sus instalaciones.
En enero del 2021, la Dirección General de Medicamentos, Insumos y Drogas (Digemid) del Ministerio de Salud le otorgó la autorización excepcional para la comercialización del kit solo durante el periodo de emergencia sanitaria y, previamente, le concedió la certificación de Buenas Prácticas en Manufactura (BPM) para la fabricación en escala industrial del innovador producto.
Esto les permitió continuar con un estudio en las regiones Amazonas, Tumbes y Lima para validar a mayor escala el kit y presentar la documentación requerida ante la Digemid para obtener el registro sanitario.
PLANES DE EXPORTACIÓN
Ahora CavBio ya cuenta con el registro sanitario otorgado por dependencia, con lo cual toda la documentación técnica concerniente al kit ha sido verificada y autorizada por la autoridad sanitaria nacional, en el marco de la reglamentación vigente, y es válido por un período de cinco años.
Con este otorgamiento, BTS Consultores logra cumplir el objetivo final de obtener una innovación debidamente acreditada por la autoridad nacional para iniciar los trámites para la exportación del kit CavBio a otros países de la región y, de esta manera, seguir contribuyendo a mitigar la pandemia causada por la covid-19.